医疗器械不良事件是指已上市的医疗器械,在正常使用情况下发生的,导致或者可能导致人体伤害的各种有害事件。我们对它的监测指的是对可疑医疗器械不良事件的发现、报告、评价和控制的一个过程。
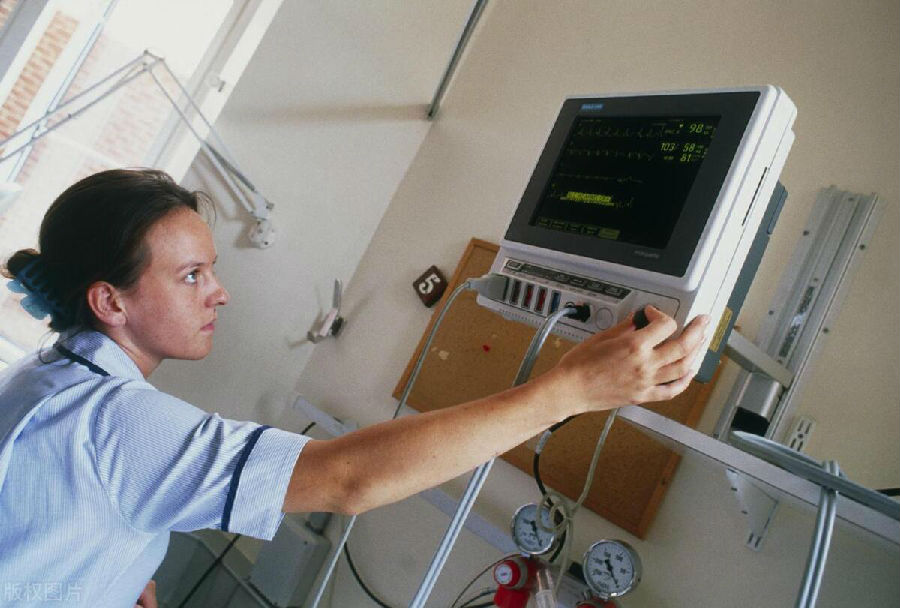
《医疗器械监督管理条例》对不良事件管理的具体要求
第五章不良事件的处理与医疗器械的召回
第六十一条 国家建立医疗器械不良事件监测制度,对医疗器械不良事件及时进行收集、分析、评价、控制。
第六十二条 医疗器械注册人、备案人应当建立医疗器械不良事件监测体系,配备与其产品相适应的不良事件监测机构和人员,对其产品主动开展不良事件监测,并按照国务院药品监督管理部门的规定,向医疗器械不良事件监测技术机构报告调查、分析、评价、产品风险控制等情况。
医疗器械生产经营企业、使用单位应当协助医疗器械注册人、备案人对所生产经营或者使用的医疗器械开展不良事件监测;发现医疗器械不良事件或者可疑不良事件,应当按照国务院药品监督管理部门的规定,向医疗器械不良事件监测技术机构报告。其他单位和个人发现医疗器械不良事件或者可疑不良事件,有权向负责药品监督管理的部门或者医疗器械不良事件监测技术机构报告。
《医疗器械临床使用管理办法》
第五章 使用安全事件处理
第三十六条 医疗机构应当对医疗器械使用安全事件进行收集、分析、评价及控制,遵循可疑即报的原则及时报告。
第三十七条 发生或者发现医疗器械使用安全事件或者可疑医疗器械使用安全事件时,医疗机构及其医务人员应当立即采取有效措施,避免或者减轻对患者身体健康的损害,防止损害扩大,并向所在地县级卫生健康主管部门报告。
第三十九条 县级及设区的市级卫生健康主管部门获知医疗机构医疗器械使用安全事件或者可疑医疗器械使用安全事件后,应当进行核实,必要时应当进行调查;对医疗机构医疗器械使用行为导致或者可能导致患者死亡、残疾或者二人以上人身损害的,应当进行现场调查,并将调查结果逐级上报至省级卫生健康主管部门。
对卫生健康主管部门开展的医疗器械使用安全事件调查,医疗机构应当配合。
医疗器械不良事件上报的目的及监测意义
一、上报目的
1.安全预警:医疗器械不良事件上报制度的主要目的是进行安全预警。一旦出现与医疗器械相关的不良事件,需要对所有使用该器械的人员提出警告,以避免医疗质量和患者安全受到更大的损害。
2.责任追溯:上报不良事件有助于追查事件原因,明确是生产问题、设计问题还是其他问题,从而采取相应的纠正措施。
3.监管支持:上报的数据为医疗器械监督管理部门提供了监管依据,有助于他们更好地了解市场动态和产品质量,进而制定更有效的监管政策。
二、监测意义
1.提高产品安全性:通过对医疗器械不良事件的监测,可以及时发现和识别上市后医疗器械存在的不合理风险,对存在安全隐患的医疗器械采取有效的控制措施,从而提高产品的安全性。
2.保障公众用械安全:监测和评价医疗器械不良事件,有助于减少或避免同类不良事件的重复发生,从而保障公众用械安全。
3.促进医务人员科学用械:医疗器械不良事件监测可以促进医务人员更加科学、合理地使用医疗器械,规范医疗操作行为,降低患者、医务人员和其他人员因使用医疗器械而造成伤害的风险。
4.推动产业发展:医疗器械不良事件监测还可以进一步提高对医疗器械性能和功能的要求,提高医疗器械相关标准,推进企业对新产品的研制和推广,有利于促进我国医疗器械产业的持续、健康发展。
综上所述,医疗器械不良事件上报和监测对于保障公众用械安全、提高产品质量、促进医务人员科学用械以及推动产业发展等方面都具有重要意义。因此,医疗机构和医务人员应高度重视医疗器械不良事件的上报和监测工作,确保医疗器械的安全、有效使用。
保力医疗器械不良事件管理解决方案
不良事件模块是保力软件的重要组成部分,旨在及时发现、记录和处理医院设备使用过程中发生的不良事件,确保设备的安全运行和患者的生命安全。通过该模块,医院能够建立起一套完善的不良事件管理机制,提高设备使用的安全性和可靠性。
